Породообразующие минералы
Классификация главнейших породообразующих минералов

Классификация главнейших породообразующих минералов основывается на их химическом составе и кристаллической структуре вещества. В настоящее время доказана взаимосвязь между химическим составом, физическими свойствами и кристаллическим строением вещества. По химическому составу и кристаллическому строению все известные минералы разделяются на несколько надклассов и классов. Важнейшими классами являются следующие:
- самородные элементы,
- сульфиды,
- оксиды и гидроксиды,
- галогенные соединения,
- углеродистые соединения
В состав надкласса соли кислородных кислот входят следующие классы: карбонаты, сульфаты, фосфаты, силикаты. Из общего числа минералов около 34% приходится на силикаты, около 25% — на оксиды и гидроксиды, около 20% — на сульфиды; на долю всех остальных минералов приходится около 21%.
Самородные элементы
К классу самородных элементов относятся платина, золото, серебро, алмаз, графит, сера, медь и др. Минералы эти состоят из одного химического элемента или смеси двух элементов, они не пользуются широким распространением (кроме графита и серы), но чрезвычайно важны в практическом отношении. К собственно породообразующим минералам можно отнести графит.

Графит
Сульфиды

Пирит
Сульфиды, или сернистые соединения элементов, в основном тяжелых металлов, не являются породообразующими минералами, но представляют большой интерес как руды цветных и черных металлов. Из сернистых минералов в земной коре наиболее широко развит пирит FeS2 (серный или железный колчедан). Аналогичен по составу марказит, отличающийся от пирита кристаллографической сингонией.
Из других минералов класса сульфидов наиболее часто встречаются халькопирит CuFeS2, галенит PbS, являющийся важнейшей свинцовой рудой, и сфалерит ZnS – цинковая руда.

Халькопирит

Галенит

Сфалерит
Оксиды и гидроксиды
Минералы класса оксидов и гидроксидов представляют собой соединения элементов с кислородом и гидроксогруппой ОН. Они широко развиты в земной коре.

Оксиды и гидроксиды (SiO2, SiO2 . H2O, MexOy, Mex(OH)y) – кремнезем, кварц, опал, магнетит, гематит, корунд и др, всего около 200

Кремнезем
В наибольшем количестве в земной коре (литосфере) содержится свободный кремниевый ангидрид или кремнезем SiO2. В состав большинства минералов он входит в виде силикатов – химических соединений с основными окислами.
Кремнезём (диоксид кремния, SiO2; лат. silica) — оксид кремния (IV). Бесцветные кристаллы с температурой плавления+1713…+1728 °C, обладающие высокой твёрдостью и прочностью.
Диоксид кремния — главный компонент почти всех земных горных пород, в частности, кизельгура. Из кремнезёма и силикатов состоит 87 % массы литосферы. В крови и плазме человека концентрация кремнезёма составляет 0,001 % по массе.

кремнезем
Свободный природный кристаллический кремнезем встречается в виде кварца – одного из более распространенных в земной коре минералов. Его кристаллы имеют форму шестигранных призм с шестигранными же пирамидами на концах.
Кварц обычно непрозрачен, чаще белого молочного цвета. Спайность кварца отсутствует. С щелочами при обычной температуре не взаимодействует, но в среде насыщенного пара или при Т=150-200 оС он вступает с Ca(OH)2 в реакцию, образуя гидросиликаты. Этим свойством кварца пользуются для получения искусственных материалов из смеси кварцевого песка и извести. Кварц имеет высокую прочность. Истинная плотность кварца 2,65 г/см3; твердость 7 по шкале твердости. Кварц имеет высокую прочность при сжатии (около 2х103 МПа) и хорошо сопротивляется действию истирания. При повышении температуры кварц претерпевает физические изменения. Так, при Т=575 оС кварц из ![]() — модификации переходит в
— модификации переходит в ![]() — модификацию, скачкообразно увеличиваясь в объеме примерно на 1,5%.
— модификацию, скачкообразно увеличиваясь в объеме примерно на 1,5%.

Кварц
При Т=870 оС ![]() — модификация начинает переходить в тридимит (плотность 2,26), значительно увеличиваясь в объеме.
— модификация начинает переходить в тридимит (плотность 2,26), значительно увеличиваясь в объеме.
Все температурные превращения кварца можно представить схемой
![]()
Кварц SiO2 – один из самых распространенных минералов. Формально по химическому составу кварц отнесен к оксидам, однако в структурном отношении он может быть причислен к подклассу силикатов с каркасной структурой.
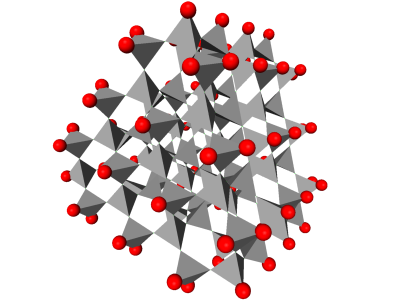
Элемент кварцевой сетки. Каждый тетраэдр представляет собой двуокись кремния SiO4. Единичные тетраэдры соединяют, разделяя атомы кислорода по своим вершинам. Красные сферы визуализируют неразделенные атомы кислорода

Анаглифическая визуализация кристалла кварца
Белый, серый, мутный или совершенно непрозрачный жильный кварц служит наряду с полевым шпатом – сырьем для производства фарфора, фаянса и огнеупорных изделий, а также применяется в качестве прибавки при плавке руд (облегчает плавку и уходит в шлак).
Кварц находится в природе в виде самостоятельной горной породы, при этом различают следующие важнейшие разновидности кварца: кварцевых песков, горный хрусталь (прозрачный, без примесей), встречающийся в виде хорошо образованных кристаллов; аметист (лилового или фиолетового цвета); топаз (буровато-дымчатого цвета); сапфир (синеватого цвета); морион (коричнево-черный прозрачный и полупрозрачный); халцедон (скрытокристаллический); агат (полосчатый халцедон). Наряду с этим кварц может входить в состав полиминеральных горных пород.

кварцевый песок

горный хрусталь

аметист


топаз

сапфир

морион

агат

халцедон
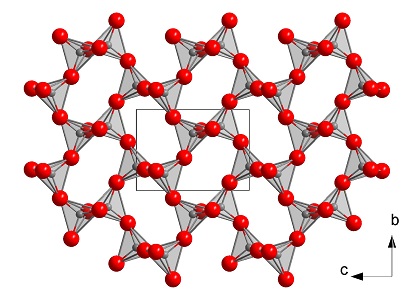
структура халцедона
Халцедон образуется из поствулканических гидротермальных растворов в базальтах, андезитах, реже в риолитах вместе с цеолитами, аметистом, кальцитом. В корах выветривания, при катагенезе карбонатных отложений.
Встречается в виде сферолитовых корок с почковидной поверхностью, отдельных желваков, конкреций, прожилок. На поперечном сколе этих образований иногда можно видеть тонкополосчатую текстуру с удлинением волокон, перпендикулярным полосчатости. В почковидных корках и отдельных сферолитах волокна халцедона обычно направлены перпендикулярно поверхности агрегатов и имеют сложную веерообразную структуру. Микроскопические волокна халцедона образуют параллельные срастания, индивидуальные волокна группируются в пучки толщиной от нескольких микрон до 50 мкм. В жеодах толщина слоёв может достигать нескольких сантиметров.


кварцевое стекло
При температуре 1710° С кварц переходит в жидкое состояние. При быстром остывании расплавленной массы (расплава) образуется кварцевое стекло — аморфный кремнезем с удельным весом 2,3. В природе встречается минерал опал аморфной структуры,’ представляющий собой гидрат кремнезема (SiO2×nH2O). Аморфный кремнезем активен, может соединяться с известью при нормальной температуре, тогда как кристаллический кремнезем (кварц) приобретает эту способность только под действием пара большого давления (в автоклаве) или при сплавлении.
Большое значение имеют оксиды и гидроксиды железа. Они являются главными минералами железных руд.
Гематит FeО3 в виде хорошо развитых кристаллов называется железным блеском, а в скрыто кристаллической форме – красным железняком.

Гематит
Магнитный железняк – магнетит Fe3O4, или FeO.Fe2O3 – оксид, наиболее богатый железом.

магнетит
Очень широко распространен бурый железняк или лимонит Fe2O3.nH2O, представляющий собой смесь различных гидроксидов железа гётита, гидрогётита и др.

лимонит

гётит

гидрогётит
К этому же классу относятся несколько разновидностей более редких минералов, из которых следует отметить корунд Аl2О3.
Корунд — один из наиболее твердых минералов. Его используют для производства высокоогнеупорных материалов, ои является ценным абразивом.
Красная разновидность корунда называется рубином, синяя – сапфиром. Гидроксид алюминия – гиббсит Al(ОН)3 входит в состав алюминиевых руд – бокситов – и иногда содержится в глинах.

корунд

рубин

сапфир

гиббсит
Второе место после кремнезема занимает в земной коре глинозем Al2O3. Свободный глинозем в природе встречается в виде минералов корунда и других глиноземистых минералов.
Другой глиноземистый материал —диаспор представляет моногидрат глинозема А12О3 • Н2О и содержит 85% А12Оз. Диаспор входит в состав бокситов — тонкодисперсных горных пород часто красного или фиолетового цвета, богатых глиноземом (от 40 до 80%) и используемых как сырье для производства глиноземистого цемента.
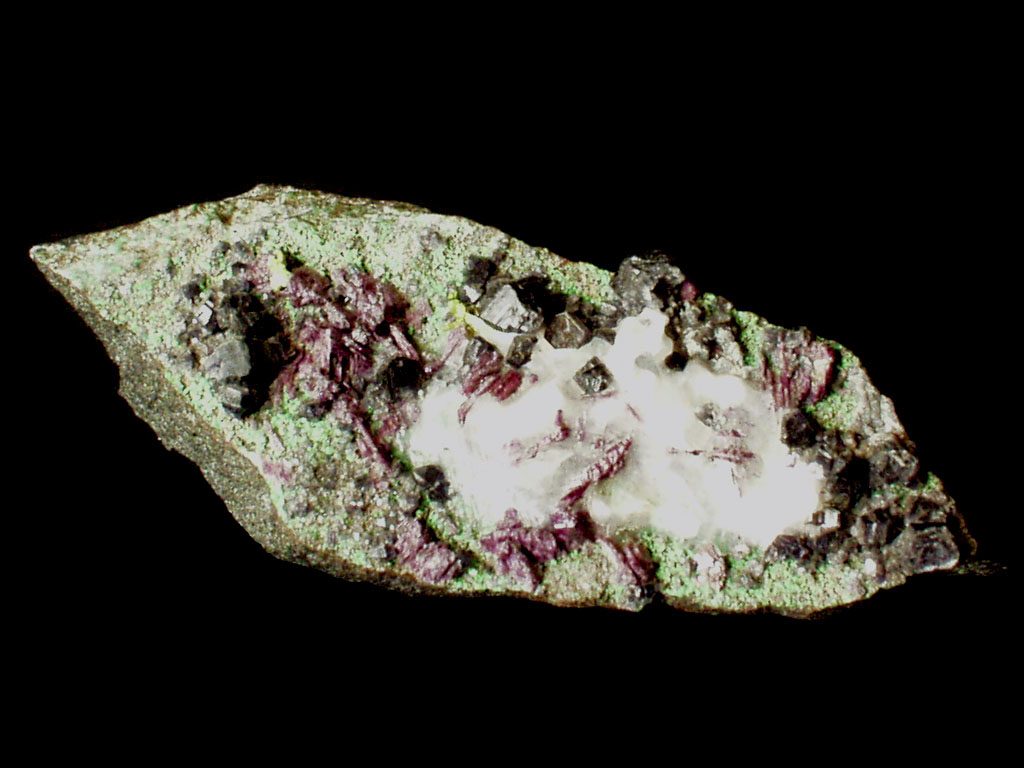
диаспор
Глинозем обычно находится в виде химических соединений с кремнеземом и другими окислами, называемых алюмосиликатами. Наиболее распространенными в земной коре алюмосиликатами являются полевые шпаты, которые составляют по весу более половины всей массы литосферы. К этой же группе минералов относятся слюды и каолиниты.

Глинозем
Полевые шпаты. Характерная особенность всех полевых шпатов — хорошо выраженная спайность по двум направлениям. В зависимости от угла, под которым пересекаются направления спайности (прямой или близкий к нему), различают ортоклаз или калиевый полевой шпат КгО • А12О3 • 6SiO2 и плагиоклазы. Последние подразделяются на альбит или натриевый полевой шпат Na2O А!2О3 • 6SiO2 и анортит или кальциевый полевой шпат СаО • А12О3 • 2SiO2.
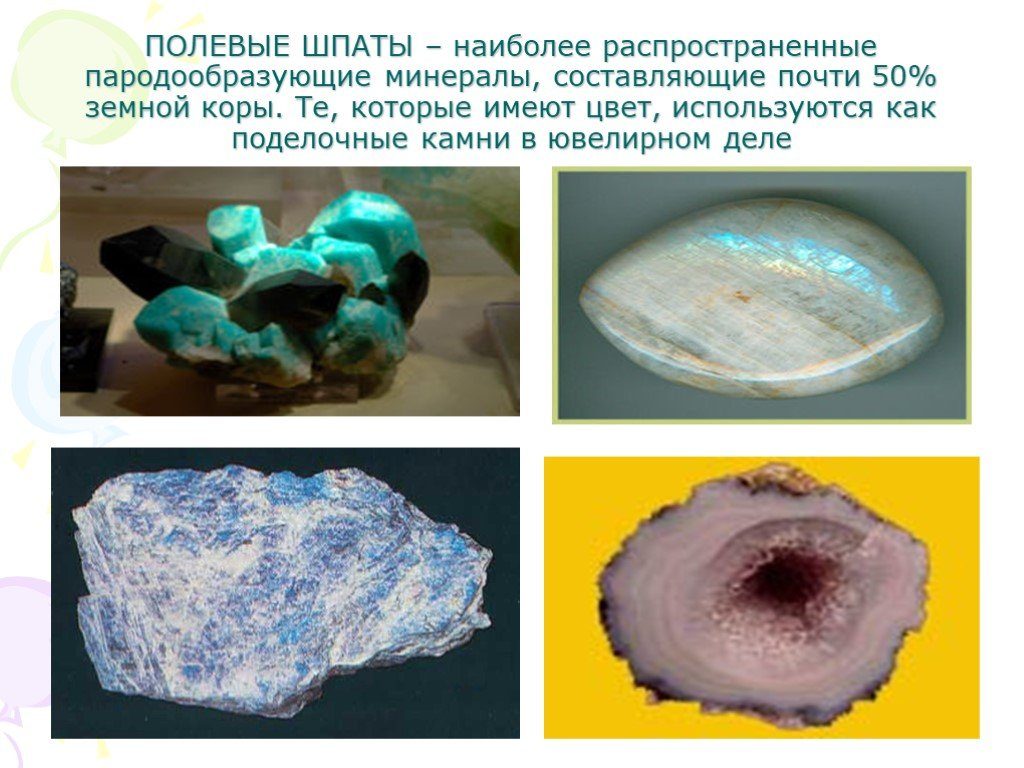

плагиоклазы

анортит
Полевые шпаты имеют цвет белый, розовый (до темно-красного), серый, желтоватый и др., удельный вес их 2,55—2,76, твердость по шкале твердости 6, прочность во много раз меньше прочности кварца (на сжатие от 1200 до 1700 кГ/см2). Стойкость полевых шпатов против механического и химического выветривания незначительна; плавятся они при температуре от 1170 до 1550° С.

Каолинит или водный алюмосиликат А12О3 • 2SiO2 • 2Н2О представляет собой продукт выветривания изверженных и метаморфических горных пород. Каолинит обычно встречается в виде белых или окрашенных рыхлых землистых или плотных масс, является основной частью глин. Удельный вес каолинита 2,6, твердость 1.

Каолинит
Галогенные соединения
Соли галогеноводородных кислот образуют около 100 минералов. Их роль как породообразующих минералов невелика, но они важны в общегеологическом и практическом отношении. Наиболее распространены из минералов этого класса хлористые соединения.

Галит
Галит (каменная соль) NaСl часто встречается среди осадочных образований озер и морей.

сильвин
К галогенным минералам относятся также сильвин KCl и флюорит CaF2. Сильвин применяется как удобрение, а флюорит – в металлургии при плавке металлов, в стекольной и химической промышленности для получения плавиковой кислоты и криолита. Прозрачные разности флюорита используются в оптике.

флюорит
Надкласс солей кислородных кислот
В этот надкласс входят соли угольной (карбонаты), серной (сульфаты), фосфорной (фосфаты) и кремниевых (силикаты) кислот выделяемые в отдельные классы.
Карбонаты
В осадочных горных породах наиболее часто встречаются породообразующие карбонатные минералы (карбонаты). Карбонаты очень широко распространены в верхних частях земной коры. К ним относятся кальцит, магнезит, доломит, сидерит другие минералы.
Кальцит, или кристаллический известковый шпат СаСОз, один из самых распространенных минералов земной коры. Он легко раскалывается по плоскостям спайности по трем направлениям, имеет удельный вес 2,7 и твердость 3. Кальцит слабо растворим в чистой воде (0,03 г в 1 л), Но растворимость его резко возрастает при содержании в воде агрессивной двуокиси углерода СО2, так как образуется кислый углекислый кальций Са(НСОз)2, растворимость которого почти в 100 раз больше, чем кальцита.

Кальцит
Кальцит, или известковый шпат, СаСО3 – один из самых распространенных минералов. Его прозрачная разновидность – исландский шпат – встречается реже и применяется в оптике.

исландский шпат
Магнезит, карбонат магния MgCO3, распространённый минерал. Название от области Магнесия (Фессалия, Греция), где был впервые обнаружен; известен с глубокой древности.
Также магнезитом является огнеупорный материал, состоящий из оксида магния MgO с 1—10 % примесей. Встречается большей частью в виде землистых или плотных агрегатов, обладающих скрыто-кристаллическим строением. Он тяжелее и тверже кальцита.

Магнезит
Магнезит MgCO3 и доломит CaMg(CO3)2 используются в химической промышленности для производства огнеупоров и изготовления цемента.
Состав близок теоретическому. Из примесей наибольшее значение имеет Fe; меньше Mn, Ca. Кристаллы редки. Обычно плотные разной зернистости агрегаты вплоть до фарфоровидных. Фарфоровидный магнезит часто содержит примеси опала и силикатов магния. Хрупок. Твёрдость 4—4,5, у фарфоровидного до 7 (за счёт тонкодисперсной примеси опала). Цвет белый, серый, реже желтоватый.
Встречается в гидротермальных месторождениях или в качестве продукта выветривания ультраосновных горных пород.
С разбавленными кислотами магнезит реагирует без вскипания, чем отличается от похожего на него кальцита.

Доломит
Доломит CaCO3•MgCO3 осадочная карбонатная горная порода, состоящую из минерала доломита на 95% и более. Получил название в честь французского инженера и геолога Деода де Доломьё (1750—1801), описавшего признаки доломитовых пород. По физическим свойствам близок к кальциту, но более тверд и прочен и еще меньше растворим в воде.

Сидерит
Сидерит минерал состава FeCO3, карбонат железа. Растворяется в минеральных кислотах. Сингония тригональная, дитригонально-скаленоэдрический класс симметрии. Структура типа кальцита. Состав (%): FeO — 61,1%; CO 2 — 37,9. Образует непрерывные изоморфные ряды твёрдых растворов с магнезитом и родохрозитом. Спайность совершенная по ромбоэдру. Цвет желтовато-белый, серый, красновато-коричневый, бледно-зелёный, иногда белый. Черта белая или светло-жёлтая. Блеск стеклянный. Полупрозрачный, иногда просвечивает. Излом неровный до раковистого. Хрупкий. Важная руда для получения железа, так как в составе до 48 % железа и нет серы и фосфора. Встречается в виде кристаллов — чаще ромбоэдрических с искривленными гранями, призматических, скаленоэдрических, а также в виде массивных зернистых агрегатов. Характерны скрученные (седловидные) кристаллы. В осадочных породах образует скрытокристаллические землистые массы, конкреции с примесью глинистых минералов и гидроксидов железа.
Родохрозит — марганцевый шпат, малиновый шпат — рудообразующий минерал MnCO3. Минерал также известен как роза инков. Инки считали, что родохрозит — это кровь древних правителей, превратившихся в камень.
Существуют изоморфные ряды MnCO3 — СаCO3 и MnCO3 — FeCO3. Марганец частично замещается магнием и цинком. Железосодержащие разновидности: понит и феррородохрозит. Сингония тригональная. Кристаллы толстотаблитчатые, призматические, ромбоэдрические, скаленоэдрические. Двойники по {0112} редки. Спайность совершенная по {1011}. Агрегаты: зернистые, плотные, столбчатые, шаровидные, скорлуповатые, корки. Цвет: розовый, красный, желтовато-серый, коричневый. Блеск стеклянный. Твёрдость 3,5-4. Удельный вес 3,7.

родохрозит

родохрозит

родохрозит
Все карбонаты вступают в реакцию со слабой (5-10%-ной) соляной кислотой, сопровождающуюся выделением углекислого газа. Степень интенсивности этой реакции позволяет отличать сходные по внешнему виду карбонаты.

малахит
К числу гидрокарбонатов относится малахит CuСО3.Cu(ОН)2, плотные массы которого слагают натечные почковидные агрегаты зеленого цвета. Землистые разновидности малахита (медная зелень) встречаются в песчаниках Урала, Украины и других районов.
Сульфаты
Сульфатные минералы (сульфаты), так же как и карбонаты, часто встречаются в осадочных горных породах. Из минералов этого класса широко распространен гипс CaSO4 .2Н2О, реже наблюдается ангидрит CaSO4 – безводный сульфат кальция. Искусственно обожженный гипс, а также тонкозернистые сплошные массы обыкновенного гипса называют алебастром. Иногда встречается длинно столбчатая волокнистая разновидность светлого голубоватого гипса, называемая селенитом. Для сульфатов, как и для карбонатов, характерны низкая твердость, светлая окраска и небольшая плотность. Они широко используются в медицине, химической промышленности и строительстве.

гипс
Гипс CaSO.4*2H2O типичный минерал осадочных пород. Строение его кристаллическое, иногда мелкозернистое, кристаллы пластинчатые, столбчатые, игольчатые и волокнистые. Встречается гипс преимущественно в виде сплошных зернистых, волокнистых и плотных пород вместе с глинами, сланцами, каменной солью и ангидритом.
Гипс имеет белый цвет, иногда бывает прозрачен или окрашен примесями в различные цвета. Удельный вес его 2,3, твердость 2. В воде гипс растворяется сравнительно легко при температуре 32—41° С, растворимость его в-75 раз больше, чем кальцита (0,22 г в 1 л).
Ангидрит CaSO4 имеет удельный вес 2,8—3, твердость 3—3,5; по внешнему виду похож на гипс. Залегает пластами и прожилками вместе с гипсом и каменной солью. Под действием воды ангидрит постепенно переходит в гипс, при этом объем его увеличивается.

ангидрит

алебастр

селенит
Фосфаты
Фосфаты представляют собой соли фосфорных кислот, например ортофосфат калия K3PO4. Различают ортофосфаты и конденсированные фосфаты, содержащие более одного атома P, образующие связи P—O—P.

В этот класс входит большое число минералов. Породообразующими из них являются апатит и фосфориты.

Апатит
Апатит Са5(F,Сl) [РО4]3 – наиболее распространенный минерал этого класса. (от греч. ἀπάτη «апати» — обман) — группа минералов класса фосфатов, с химической формулой Ca10(PO4)6(OH,F,Cl)2, основной компонент апатитовых руд богатых фосфором(агрономические руды).
Встречается в природе в разных видах и внешне похож на минералы берилл, диопсид или турмалин (т.е. вводит в заблуждение, с чем и связано его наименование). Основным диагностическим признаком апатита служит призматический облик кристаллов; от похожего на него берилла отличается существенно меньшей твёрдостью.

Фосфориты
Фосфориты – осадочные морские образования, близкие по составу к апатиту, содержащие примеси кварца, карбонатов, глауконита и глинистых частиц. Они обычно образуют радиально-лучистые и скрытокристаллические конкреции.
Силикаты
К классу силикатов относится наибольшее число минералов, входящих в состав земной коры. Эти минералы слагают большинство горных пород.
Установлено, что во всех силикатах каждый ион кремния Si4+ находится в соединении с четырьмя ионами кислорода и может быть изображен формулой [SiO4]4—. Основная структурная единица силикатов – кремнекислородный тетраэдр – группировка, состоящая из четырех больших ионов кислорода и одного иона кремния. При этом центры ионов кислорода образуют четыре вершины тетраэдра, а ион кремния занимает центр такого тетраэдра.
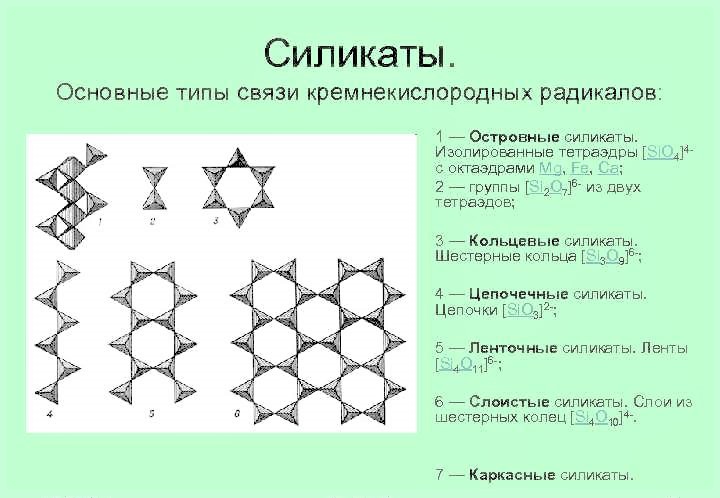
В основу классификации силикатов положен способ соединения тетраэдров. Все минералы силикатов разделяются в зависимости от способов сочленения кремнекислородных тетраэдров на следующие группы: островные, кольцевые, цепочечные, ленточные, листовые и каркасные.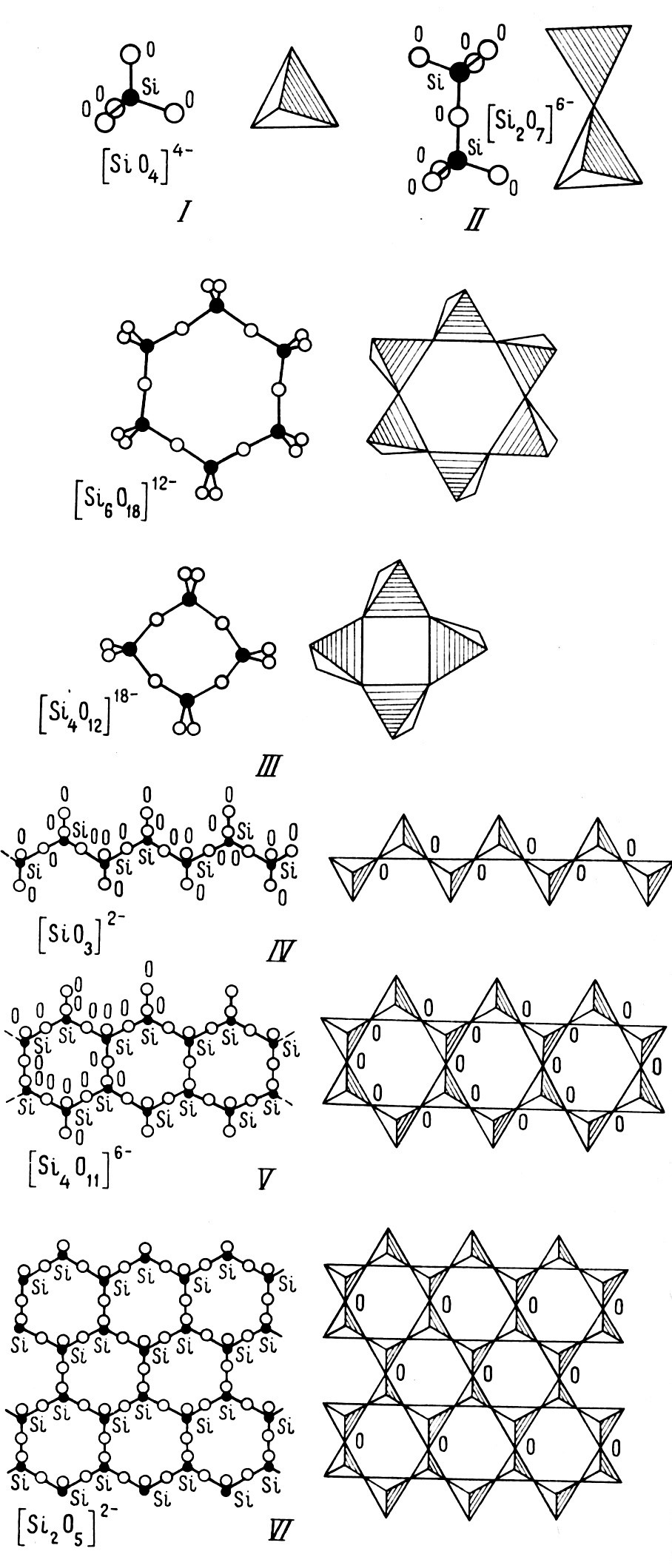
Типы соединения кремнекислородных тетраэдров: I – изолированный тетраэдр, II – группа из двух тетраэдров (сдвоенных), группы соединённых тетраэдров образующих: III – кольца, IV – цепочку, V – ленту, VI – слой (лист).
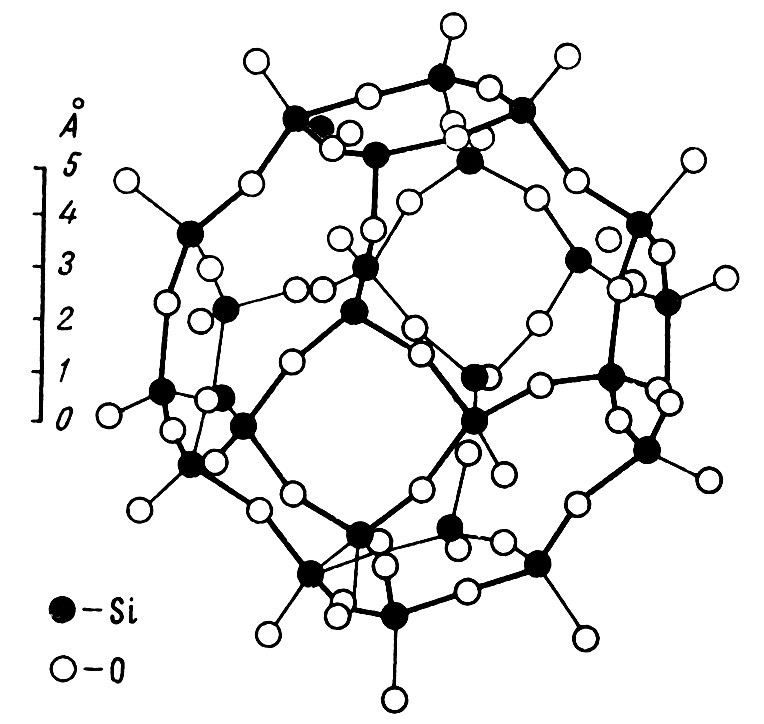
Типы соединения кремнекислородных тетраэдров: группы соединённых тетраэдров образующих каркас
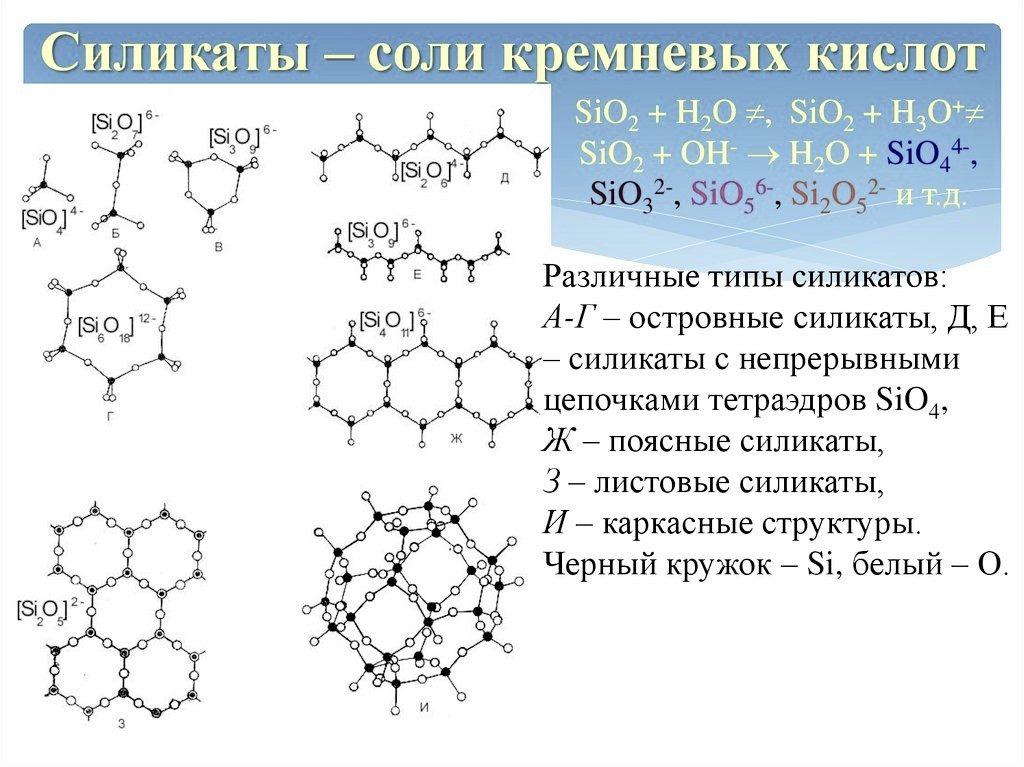

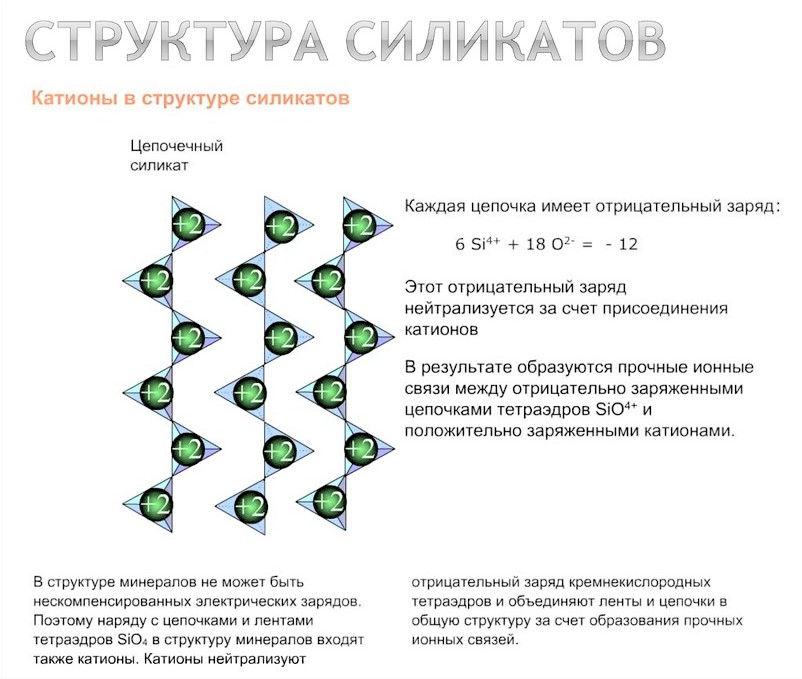
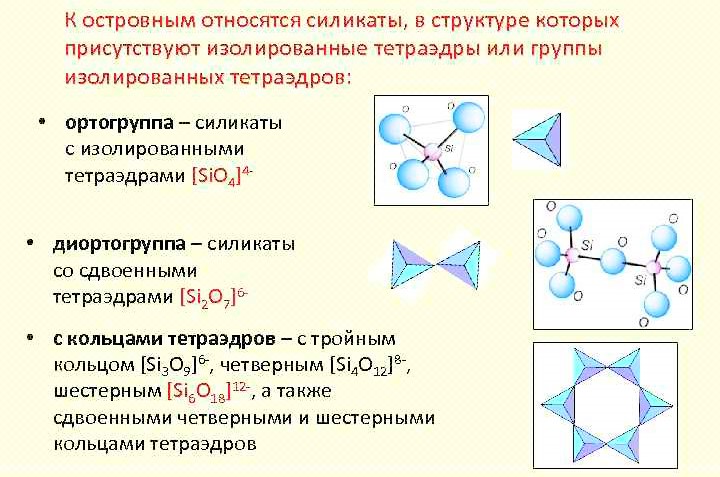
1) Островные силикаты. В структуре силикатов этой группы кремнекислородные тетраэдры не имеют общих вершин, т.е. общих ионов кислорода, и удерживаются в решетке ионами других элементов.

Оливин и гранат относятся к породообразующим минералам железисто-магнезиальной группы, являясь островными силикатами. Минералы, входящие в эту группу, имеют темную окраску, поэтому их часто называют темно-окрашенными минералами. Удельный вес их больше, чем других силикатов, твердость находится в пределах 5,5— 7,5; они обладают значительной вязкостью. При большом содержании их в горных породах они придают последним темный цвет и большую вязкость, т. е. повышенную сопротивляемость удару.

оливин
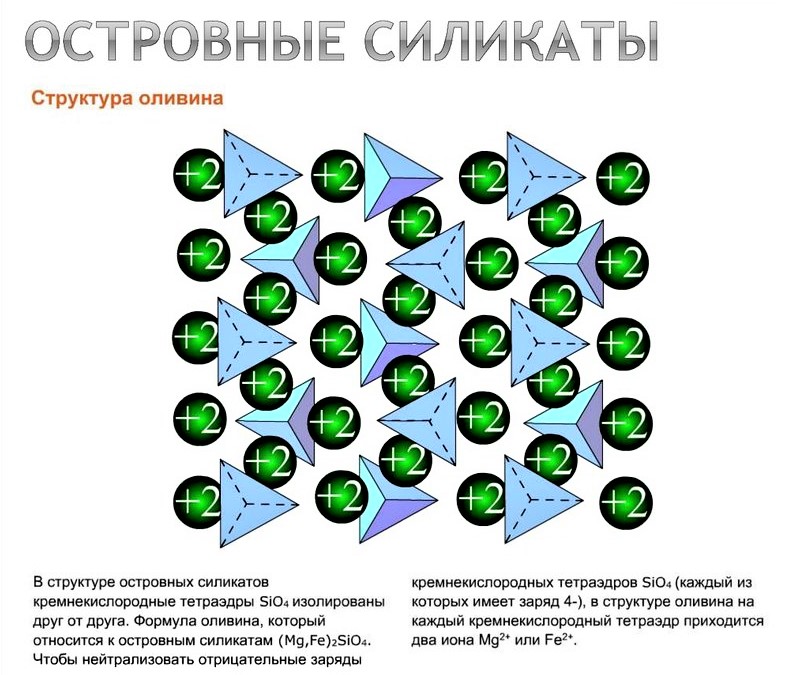
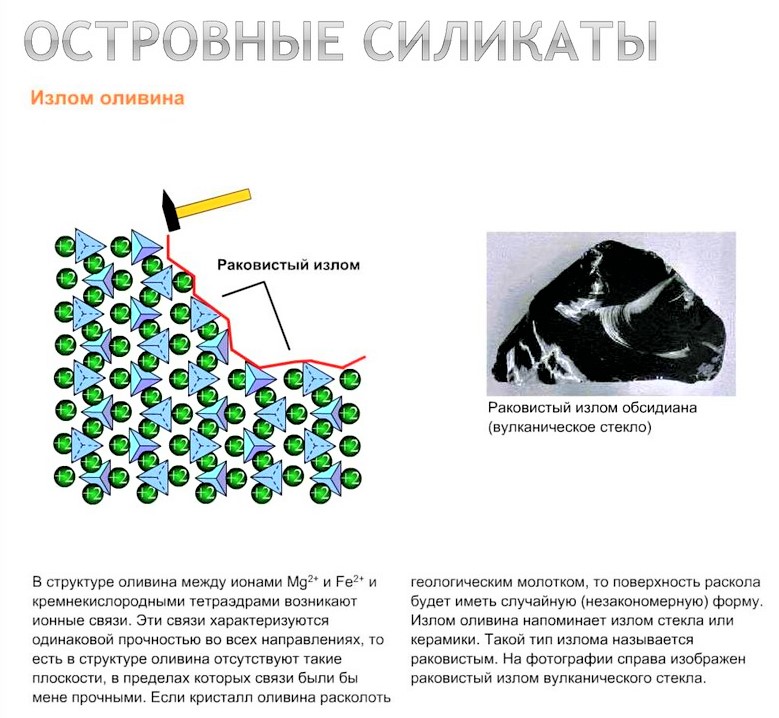
Оливин (Fe,Mg) [SiO4] – минерал зеленого цвета, железо магнезиальный, бедный кремнекислотой силикат он характерен для ультраосновных или основных изверженных пород. Встречается виде зернистого агрегата и отдельных зерен.
Оливин отличается малой стойкостью: под воздействием различных реагентов (Н2О, Ог, СО2 и др.) он изменяется и в результате присоединения воды увеличивается в объеме, переходя в змеевик или серпентин. Одна из разновидностей серпентина имеет волокнистое строение и называется хризотиласбестом, или горным льном.

хризотиласбест
Хризотиласбест состоит из тонких и прочных волокон; его широко используют в асбестоцементной промышленности и в производстве теплоизоляционных материалов. Крупные месторождения хризотиласбеста находятся на Урале. .

гранат
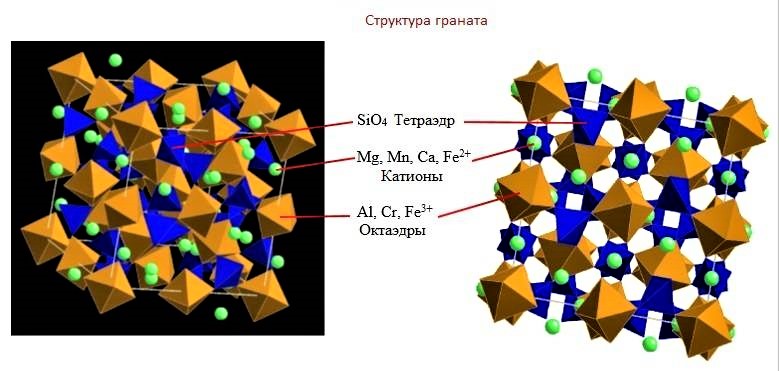
Гранаты встречаются преимущественно в метаморфических и метаморфизованных породах реже в изверженных породах. Известно несколько разновидностей гранатов, из которых самым распространенным является альмандин Fe3Al[SiO4]3 темно-красного или буроватого цвета; реже встречается розовато-красный пироп Mg3Al2 [SiO4]3 и наиболее редко – зеленый гроссуляр Са3А12 [SiO4]3
К амфиболам относится роговая обманка — типичный минерал изверженных пород — с удельным весом 3,1—3,5.
2) Кольцевые силикаты. Силикаты, структура которых образована кольцами из трех, четырех или шести кремнекислородных тетраэдров называются кольцевыми.
Представителем силикатов с кольцом из шести тетраэдров – [Si6O18] является берилл Ве2А13 [Si6O18] – полупрозрачный и прозрачный зеленый минерал, образующий шестигранные призматические кристаллы. Из него добывается металл бериллий.

берилл
К этой же группе относится турмалин – сложный бороалюмо-силикат встречающийся главным образом в гранитных породах и пегматитовых телах, а также в сланцах на границе с магматическими породами. Красиво окрашенные прозрачные разновидности турмалина используются как драгоценные камни; некоторые разновидности применяются в радиотехнике.
3) Цепочечные силикаты. В структуре силикатов этой группы кремнекислородные тетраэдры соединены в неправильные цепочки с радикалом [SiO3]2-. Цепочечные силикаты состоят из одинарных цепочек тетраэдров. В группу этих силикатов входят железо-магнезиальные силикаты семейства пироксенов, среди которых различают моноклинные и ромбические.
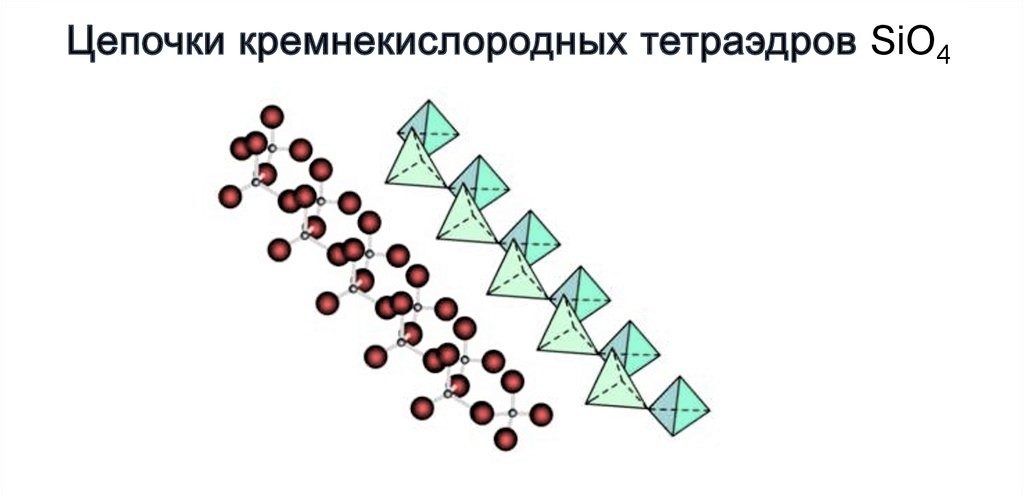
Объединение кремнекислых тетраэдров в бесконечные цепочки двумя способами: точечная и полиэндрическая модели. Каждый тетраэдр связан с другими посредством общих атомов кислорода
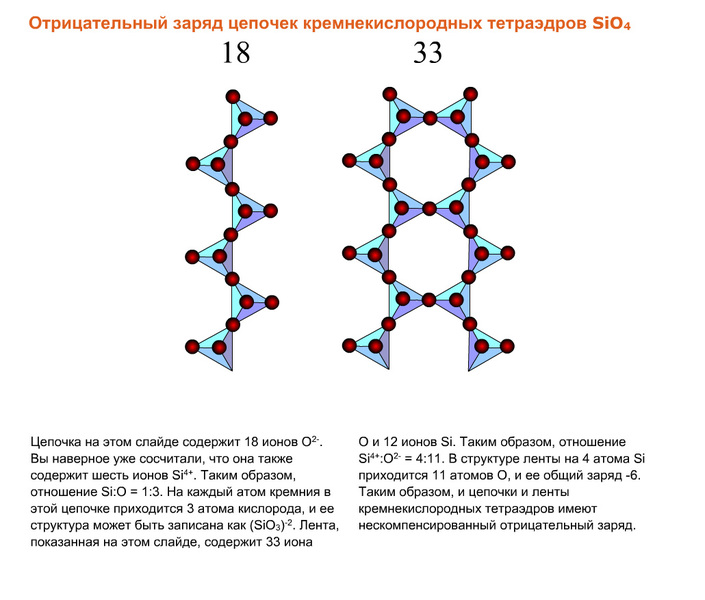
Пироксены — обширная группа цепочечных силикатов. Многие пироксены — породообразующие минералы, из семейства которых наиболее часто встречаются авгиты (глиноземистые пироксены), имеют удельный вес 3,2—3,6.

пироксены
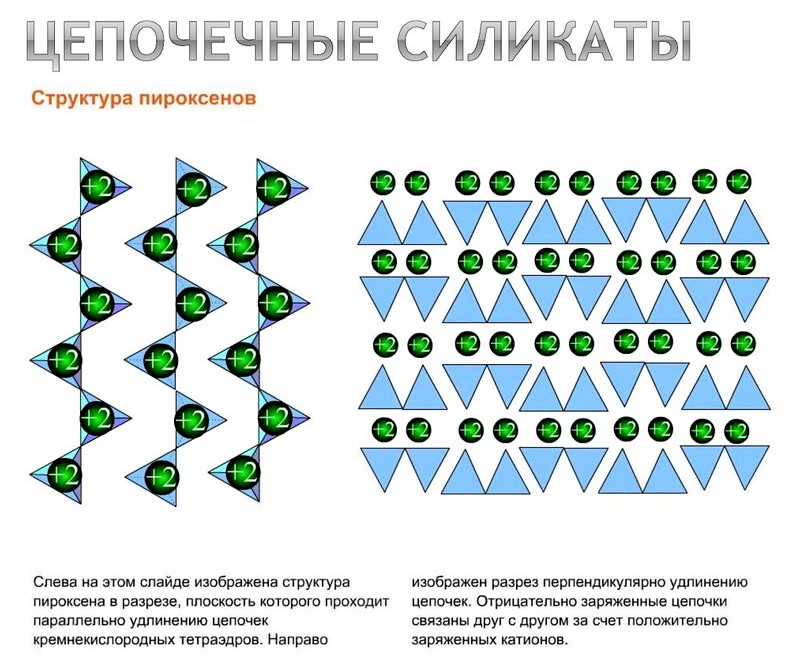
Главным мотивом структуры пироксенов являются цепочки SiO4 тетраэдров, вытянутые по оси с. В пироксенах тетраэдры в цепочках поочередно направлены в разные стороны. У других цепочечных силикатов период повторяемости цепочки обычно больше.
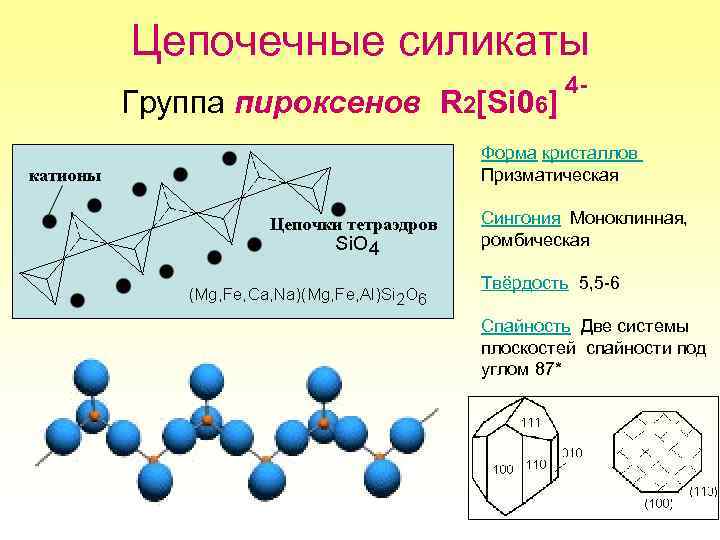
В структуре имеется две неэквивалентные позиции — М1 и М2. Позиция М1 по форме близка правильному октаэдру и в ней располагаются мелкие катионы. Позиция М2 менее правильная и при вхождении в неё крупных катионов (особенно Ca) она приобретает 8-ную координацию, кремнекислородные цепочки смещаются относительно друг друга и структура минерала становится моноклинной.

авгит
Представителем моноклинных пироксенов является авгит Са(Mg,Fe,Al)[(SiAl)2O6] – минерал сложного и непостоянного химического состава. В структуре авгита алюминий находится в центре кислородных тетраэдров, занимая место кремния. Для этого минерала характерны кристаллы зеленовато-черного цвета с восьмиугольным сечением и блестящими гранями.
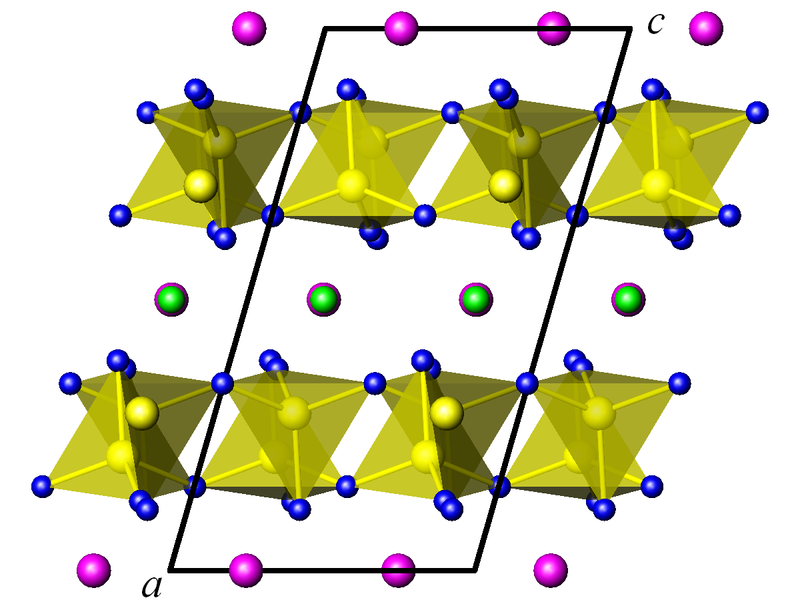
Кристаллическая структура авгита. Зеленый: кальций, розовый: магний, желтый: кремний, синий: кислород
Среди ромбических пироксенов выделяются энстатит Mg2[Si2O6]6 и гиперстен (Fe, Mg)2[Si2О6].
4) Ленточные силикаты. Наиболее распространенными представителями этих силикатов являются амфиболы, которые входят в состав магматических и метаморфических горных пород. Строение амфиболов гораздо сложнее, чем пироксенов, но между этими группами имеется много общего: цвет и облик кристаллов, твердость, плотность.
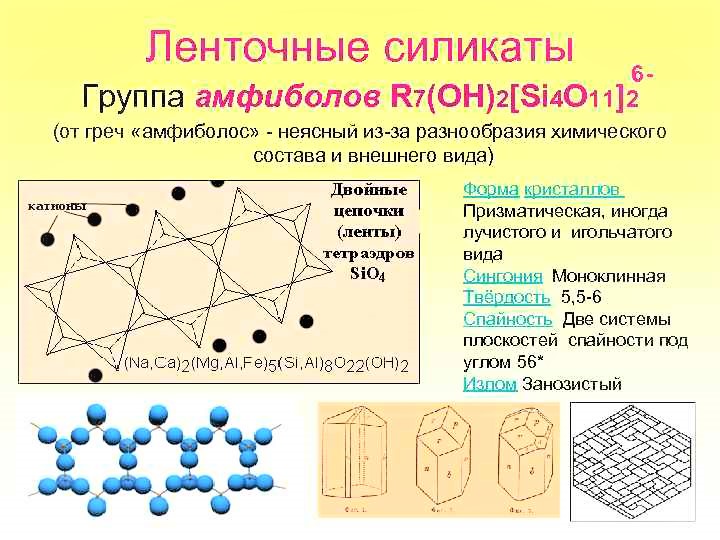
Как и пироксены, они кристаллизуются в ромбической и моноклинной сингониях. В отличие от пироксенов у большинства амфиболов шелковистый блеск, вытянутые столбчатые, часто игольчатые кристаллы шестиугольного сечения, более совершенная спайность.

амфиболы

Дианит (стронциевый амфибол)
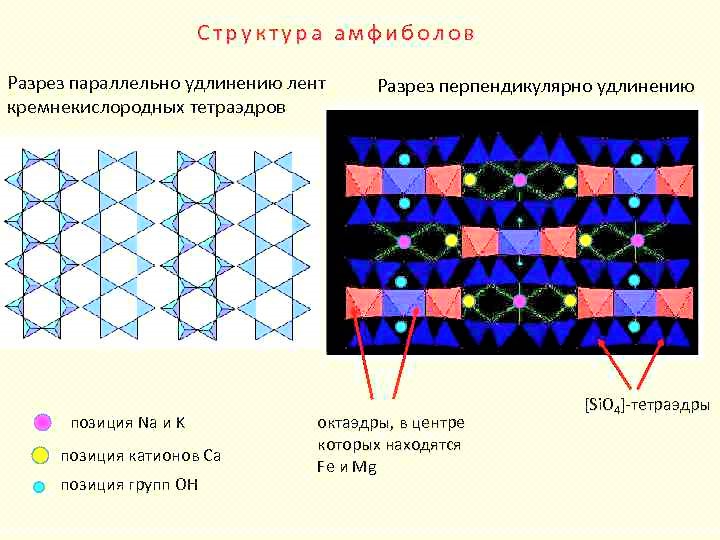

Наиболее широко развиты моноклинные амфиболы, главным образом роговая обманка. Состав ее весьма разнообразен и непостоянен: он может быть выражен формулой (Са,Na)2 (Mg,Fe2+)4(Al,Fe3+)[(Si, Al)4О11]2 (F,ОН)2. Роговая обманка имеет светло-темно-зеленый и буровато-черный цвет. От авгита она отличается волокнистостью и шелковистым блеском вытянутых столбчатых кристаллов.

Актинолит

Роговая обманка

Роговая обманка

5) Листовые (слоевые) силикаты. Если ленты тетраэдров соединяются в один непрерывный слой, то образуется структура листовых силикатов. Внутренняя структура минералов этого подкласса определяет их весьма совершенную спайность в одном направлении и небольшую твердость. В составе этих силикатов кроме Si и О присутствуют Mg, Al, К, Na и Са, а также гидроксогруппа ОН.
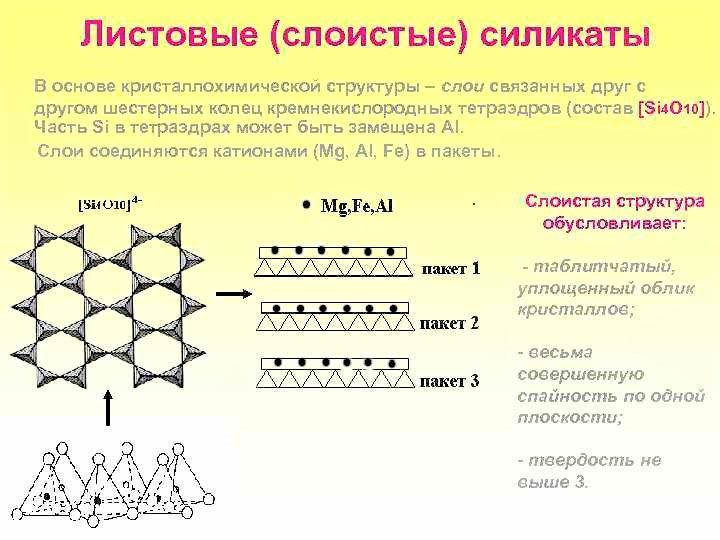
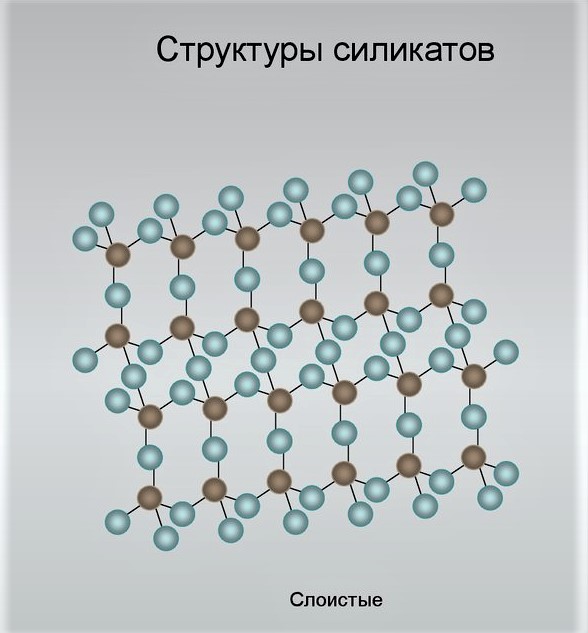
Среди листовых силикатов можно выделить силикаты и алюмосиликаты.
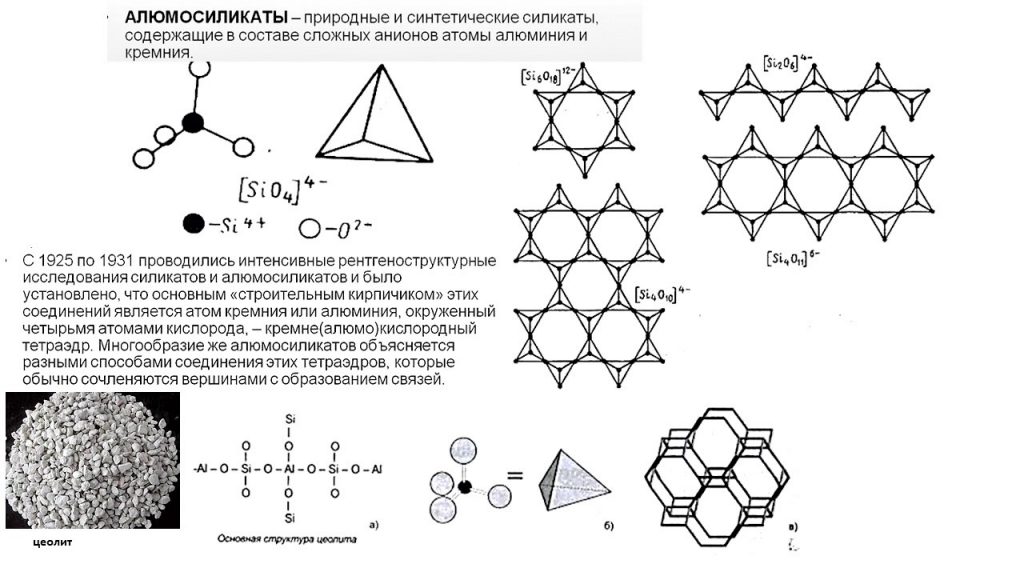
К листовым силикатам относятся тальк, серпентин и каолинит, а к листовым алюмосиликатам – слюды, хлориты и гидрослюды, из которых наиболее характерным является глауконит, образующийся в морских условиях. Листовые силикаты и алюмосиликаты являются весьма распространенными минералами изверженных и метаморфических горных пород (за исключением глауконита).

Тальк Mg3(OH)2 [Si4О10]

Серпентин
Серпентин Mg6(OH)8 [Si4O10] отличается от талька только большим содержанием магния и меньшим – кремнезема. Горная порода, состоящая из серпентина, часто называется серпентинитом, или змеевиком – по зеленой пятнистой окраске («серпенс» — змея). Широко известна волокнистая разность серпентина – асбест. Асбест используется для изготовления огнеупорных тканей, прокладок и многих других изделий.

Каолинит
Каолинит Al4(OH)8[Si4O10] формируется при химическом выветривании алюмосиликатов магматических пород на поверхности земли. Он входит в состав многих глин. Землистые рыхлые массы каолинита называются каолином. Употребляется этот минерал в строительном деле, керамическом производстве, бумажной промышленности и как огнеупорный материал.

Слюды
Слюды – листовые, водные алюмосиликаты, имеющие важное породообразующее значение. Разнообразного состава, они входят в состав многих магматических и метаморфических горных пород. Общее количество слюд в породах земной коры – около 4%. Минералы этого ряда кристаллизуются в моноклинной сингонии, обладают весьма совершенной спайностью в одном направлении, благодаря которой они расщепляются на тончайшие упругие листочки и пластинки. Твердость слюд находится в пределах 2—3 по шкале твердости.
Наиболее часто встречаются следующие виды слюд:
- калиевая (мусковит) — светлая, прозрачная (в тонких листочках), тугоплавкая, химически стойкая;
- железисто-магнезиальная (биотит)—непостоянного состава, очень темного цвета (черного, бурого), легче разрушающаяся, чем мусковит;
- вермикулит — гидрослюда золотисто-бурого цвета, образующаяся в результате окисления и гидратации биотита; при прокаливании вермикулит теряет воду и увеличивается в объеме в 18—25 раз; обожженный вермикулит (зонолит) применяется как теплоизоляционный материал.

вермикулит
Породообразующее значение имеют мусковит и биотит.

Мусковит
Мусковит KA12(OH,F) [A1SiOio] – бесцветная или слабо окрашенная желтоватая, зеленоватая прозрачная калиевая слюда.
Мусковит (от англ. muscovite — московский, московит, москвитянин) — минерал, калиевая слюда KAl2[AlSi3O10](OH)2. Ярко-зелёный мусковит, содержащий до 4 % Cr2О3, называют фукситом, мелкочешуйчатый агрегат — серицитом. Используют в электро- и радиотехнике, для изготовления смотровых оконцев в котлах, печах и др.
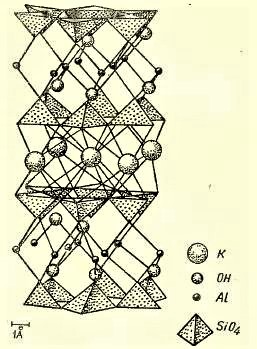
Последовательность слоев в структуре мусковита

фуксит

серицит
Название минерала связано с тем, что в Средние века основным поставщиком слюды в Европу было Русское государство, часто называемое Московия. В результате в английском языке слюда получила название «muscovy glass» — московитское стекло. Русское минералогическое название слюды — мусковит. Существуют также и другие названия минерала и его разновидностей: московская звезда, калиевая слюда, белая слюда, серицит, антонит, лейкофиллит.
Мусковит применяется как прекрасный изоляционный материал, а его порошок (скрап) служит для изготовления огнестойких строительных материалов, бумаги, красок, автомобильных шин и т. д.

Биотит
Биотит K(Mg, Fe2+, Fe3+, A1)3(OH, F)2[AlSi3O10] – магнезиально-железистая слюда зеленовато- или коричневато-черного цвета. Биотит широко распространен во многих магматических и метаморфических горных породах. Бурая магнезиальная слюда, похожая на биотит, но не ломкая, называется флогопитом. Она широко используется в электротехнике.

Хлориты
Хлориты – водные алюмосиликаты магния и железа. Название этим минералам дано по своеобразному зеленому цвету («хлорос» — зеленый). Хлориты развиты в основном в метаморфических породах, в которых они формируются за счет магнезиально-железистых силикатов. Некоторые из хлоритов содержат до 38% железа и используются как железные руды (шамозит).

Глауконит
Глауконит K(Fe3 +, Al, Fe2 +, Mg)2-3(OH)2[AlSi3O10].nH2O относится к группе гидрослюд. По данным рентгеноструктурных исследований, он является смесью нескольких минералов. Глауконит образуется в неглубоких морских бассейнах и широко распространен в песках, глинах, опоках, известняках и других осадочных породах, где встречается в виде скрыто кристаллических зернышек округлой формы. Используется как калийное удобрение в сельском хозяйстве и для смягчения жесткости воды.
6) Каркасные силикаты. От всех остальных силикатов минералы этой группы отличаются тем, что в их решетке кремния-алюмо-кислородные тетраэдры соединены друг с другом всеми четырьмя вершинами, в результате чего образуется каркас.


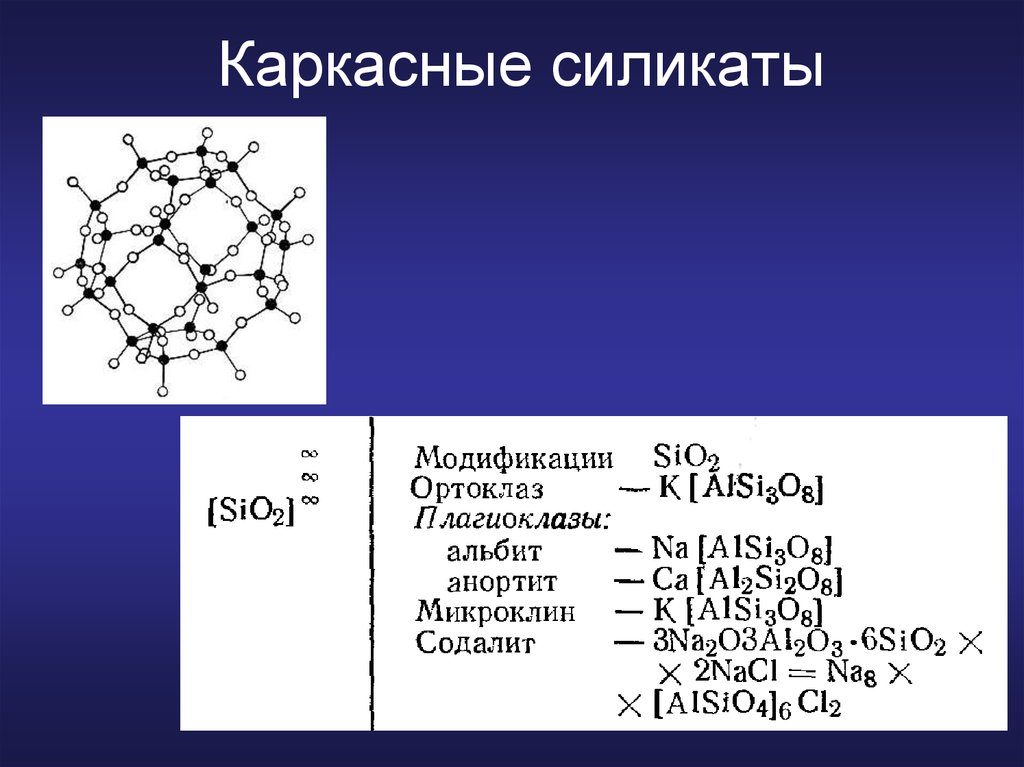

альбит

анортит
В каркасных силикатах ионы алюминия занимают место некоторых ионов кремния, и в соответствии с этим тетраэдры делятся на алюмо- и кремнекислородные. Каркасные силикаты делятся на две основные группы минералов: полевые шпаты и фельдшпатоиды.
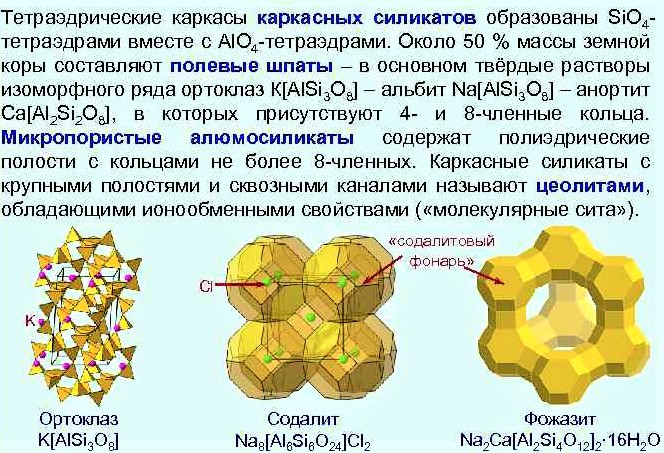

фожазит

фожазит

содалит

ортоклаз


По химическому составу среди полевых шпатов выделяются калиево-натриевые (щелочные) и известково-(кальциево)-натриевые, или плагиоклазы.
Из щелочных полевых шпатов важное значение имеет ортоклаз K[AlSi3O8] – минерал с желтовато-розовой и мясокрасной окраской, кристаллизующийся в моноклинной сингонии и образующий прямоугольные сколы по спайности в двух направлениях (от греч. «ортоклаз» — прямоколющийся). К этой же группе относится микроклин, аналогичный ортоклазу по химическому составу, но кристаллизующийся в триклинной сингонии.

ортоклаз

микроклин

Плагиоклазы по химическому составу представляют собой непрерывный ряд изоморфных смесей двух составных частей: альбитовой Ab-Na [AlSi3O8] и анортитовой An-Са [Al2Si2O8]. Плагиоклазы разного состава носят различные названия: олигоклаз, андезин, лабрадор и битовнит, в них соответственно уменьшается содержание (в %) натриевой составляющей Ab и увеличивается кальциевой An. Все плагиоклазы кристаллизуются в триклинной сингонии.

Фельдшпатоиды по химическому составу сходны с полевыми шпатами, но беднее их кремнекислотой. Они как бы замещают полевые шпаты в некоторых магматических породах, бедных кремнекислотой, но богатых щелочами, и поэтому играют существенную роль в составе щелочных пород.

Альбит, натриевый полевой шпат

нефелин, фельдшпатоид
Альбиту (натриевому полевому шпату) соответствует фельдшпатоид нефелин (Na,К) [AlSiO4]. Он входит в состав бескварцевых щелочных магматических пород – нефелиновых сиенитов – и применяется в стекольной, керамической и химической промышленности, а также используется для производства алюминия.

лейцит
Калиевым полевым шпатам (ортоклазу и микроклину) соответствует лейцит K[AlSi2O6] – породообразующий минерал излившихся пород, который может использоваться для производства калия и алюминия.
Углеродистые соединения
Углеродистые соединения существенно отличаются от многих минералов по происхождению, химическим свойствам и кристаллическому строению. К минералам, состоящим из углеводородов с некоторым количеством кислорода, можно отнести асфальт, озокерит и янтарь.

Асфальт
Асфальт – продукт окисления углеводородов нефти. В его составе основную роль играют углерод (80%), кислород (10%) и водород (10%). Это коричнево-черная мягкая масса, которая горит и легко плавится. Применяется асфальт для дорожных покрытий, в химической промышленности.

Озокерит
Озокерит (горный воск) состоит на 84% из углерода и на 16% из водорода. По внешнему виду и физическим свойствам озокерит очень сходен с воском. Он образуется при охлаждении парафиновой нефти путем кристаллизации высокомолекулярных углеводородов. Озокерит используется для получения искусственного воска – церезина, используется для пропитывания тканей и других технических и медицинских целей.

Янтарь
Янтарь С10Н16О представляет собой ископаемую древесную смолу. Это легкий аморфный минерал буровато-желтого цвета, прозрачный и полупрозрачный, с раковистым изломом и небольшой твердостью (2-2,5). Он применяется в электротехнике как изолятор, в ювелирном деле и химической промышленности.
Литература
- Бондарев В.П. Геология. Лабораторный практикум. Полевая геологическая практика: Учеб. пособие для студентов учреждений среднего профессионального образования. М.: ФОРУМ: ИНФРА-М, 2002. -190с.
- Геология: Учеб. для эколог. специальностей вузов / Н.В. Короновский, Н.А. Ясманов. –М.: Изд. Центр «Академия», 2003. -448 с.
- Основы геологии: Учеб. для географ. специальностей вузов / Н.В. Короновский, А.Ф. Якушова. –М.: Высш. шк., 1991. -416 с.
- Пособие к лабораторным занятиям по общей геологии: Учеб. пособие для вузов / В.Н. Павлинов, А.Е. Михайлов, Д.С. Кизевальтер и др. – 4-е изд., перераб. и доп. –М.:Недра, 1988. -149 с.: ил.
- Силикаты природные